První termodynamický zákon vyjadřující princip zachování energie (viz čl. 3.2) vylučuje existenci perpetua mobile prvního druhu - zařízení, které by trvale získávalo mechanickou energii, aniž by k tomu spotřebovalo ekvivalentně jiný druh energie. Podle prvního termodynamického zákona však není vyloučena možnost existence periodicky pracujícího stroje, který by veškeré teplo Q odebrané z ohřívače využil k vykonání práce W' = Q. Výsledek Carnotova ideálního
kruhového děje však ukazuje, že vykonává práce W' pracovní látky v důsledku přijetí tepla Q1 od ohřívače je nutně doprovázena odevzdáním tepla Q'2 < Q1 do chladnější lázně. K získání práce je bezpodmínečně nutná existence dvou lázní různých teplot. Schematicky je tato skutečnost znázorněna na obr. 4-3. Podobně každý jiný tepelný motor pracuje v podstatě jako motor s Carnotovým cyklem. Přijímá teplo od teplejších těles, část z něho transformuje v práci a zbytek předává chladnějším tělesům.
Uvažme nyní Carnotův kruhový děj v obráceném směru, než jsme uvažovali v čl. 4.2. Tento obrácený (nepřímý) Carnotův cyklus můžeme sledovat z obr. 4-4. Vyjdeme z počátečního stavu znázorněného bodem A. Plyn adiabaticky expanduje (A
 D), až jeho teplota klesne z T1 na T2 (stav D). Při teplotě T2 plyn izotermicky expanduje (D
D), až jeho teplota klesne z T1 na T2 (stav D). Při teplotě T2 plyn izotermicky expanduje (D
 C) a přitom odebere z chladiče teplo Q2. Ze stavu C do stavu B je plyn adiabaticky stlačován vnějšími silami, přičemž jeho teplota vzroste z T2 na T1 Cyklus se uzavře izotermickou kompresí (B
C) a přitom odebere z chladiče teplo Q2. Ze stavu C do stavu B je plyn adiabaticky stlačován vnějšími silami, přičemž jeho teplota vzroste z T2 na T1 Cyklus se uzavře izotermickou kompresí (B
 A), při níž plyn odevzdá teplejší lázni teplo Q'1.
A), při níž plyn odevzdá teplejší lázni teplo Q'1.
 Obr. 4-5
Obr. 4-5
Výpočty energetické bilance jsou obdobné jako při přímém cyklu. Výsledkem je poznatek, že plyn odebírá z chladiče teplo Q2 , z vnějšku je na něm vykonána práce W a ohřívači odevzdá teplo Q'1 (obr. 4-5), při čemž platí
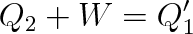 |
Na tomto principu jsou založeny chladicí zařízení . Podstatné však je to, že převod tepla z chladnější lázně do lázně teplejší je možný jen vykonáním vnější práce.
Princip vratného Carnotova cyklického děje představuje přechod od prvního termodynamického zákona k druhému termodynamickému zákonu. Lze ho vyslovit různě:
Clausiova formulace z roku 1850 (Clausiův princip):
Teplo nemůže samovolně přejít z tělesa studenějšího na těleso teplejší. Kelvinova formulace (z roku 1851):
Je nemožné získat ze soustavy neživých látek kruhovým dějem práci jen tím způsobem, že by se nějaká látka ochlazovala na teplotu nižší než je teplota nejstudenějšího místa v okolí.
Thompson a Planck zevšeobecnili poznatek o ideálním Carnotově kruhovém ději a formulovali druhý termodynamický zákon takto (Thompsonův princip):
Není možné sestrojit periodicky pracující stroj, který by nezpůsoboval nic jiného, než že by trvale ochlazoval zvolenou tepelnou lázeň a konal rovnocenou práci.
W. Ostwald (Němec, 1853-1932) takový stroj nazval perpetuum mobile druhého druhu, a tak formuloval druhý termodynamický zákon krátce výrokem:
Není možně sestrojit perpetuum mobile druhého druhu.
Z druhého termodynamického zákona vyplývají dvě Carnotovy věty týkající se účinnosti Carnotových cyklů.
1. První věta Carnotova: Účinnosti všech vratných Carnotových cyklů pracujících s týmiž lázněmi jsou stejné a závisí jen na teplotách obou lázní.
2. Druhá Carnotova věta: Účinnost libovolného nevratného Carnotova cyklu není nikdy větší než účinnost Carnotova cyklu vratného, který pracuje mezi týmiž teplotami jako cyklus nevratný.