Model plynu, který používá kinetická teorie , je možno využít při výpočtu koeficientů transportních jevů. Zřejmě bude transportní jev probíhat tím rychleji, čím intenzivnější bude tepelný pohyb molekul. Mírou intenzity pohybu molekul může být např. střední rychlost molekul. Transportní jev však nebude probíhat rychlostí srovnatelnou se střední rychlostí molekul. Příčinou je existence vzájemných srážek molekul. Při nich se náhodně mění směr pohybu molekul, takže trajektorie molekul nejsou zdaleka přímočaré. Počet srážek za jednotku času, tzv. srážková frekvence, může tedy ovlivnit hodnotu transportního koeficientu. Stanovíme proto nejprve průměrnou hodnotu srážkové frekvence.
Ve vyšetřovaném plynu objemu V nechť je N molekul, neboli hustota molekul je NV = N/V Budeme předpokládat, že všechny molekuly jsou kulového tvaru
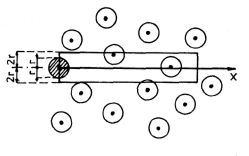 Obr. 6-2
Obr. 6-2
o stejném poloměru r, a až na jednu molekulu, jež se pohybuje směrem osy x, jsou ostatní v klidu (obr. 6-2). Tato molekula (na obr. 6-2 vyšrafovaná) narazí při svém pohybu za jednotku času na všechny molekuly, jejichž středy leží ve válci, který má poloměr 2r a jehož osa ztotožňující se se směrem osy x má délku h, číselně rovnou střední rychlosti
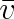 pohybující se molekuly. Předpokládejme ještě, že srážkou této molekuly s ostatními stojícími molekulami se směr jejího pohybu nezmění. Poněvadž objem uvažovaného válce je
pohybující se molekuly. Předpokládejme ještě, že srážkou této molekuly s ostatními stojícími molekulami se směr jejího pohybu nezmění. Poněvadž objem uvažovaného válce je
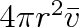 , platí pro střední počet srážek z za jednotku času dané molekuly s ostatními vztah
, platí pro střední počet srážek z za jednotku času dané molekuly s ostatními vztah
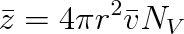 |
(6.4) |
Výraz
 vyjadřuje obsah plochy, ve které se musí nacházet středy obou molekul, aby došlo ke srážce. Pro označení obsahu této plochy se používá obecně název účinný srážkový průřez, označíme jej symbolem
vyjadřuje obsah plochy, ve které se musí nacházet středy obou molekul, aby došlo ke srážce. Pro označení obsahu této plochy se používá obecně název účinný srážkový průřez, označíme jej symbolem
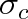 . Srážkovou frekvenci pak bude vyjadřovat vztah
. Srážkovou frekvenci pak bude vyjadřovat vztah
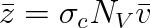 |
(6.5) |
Za normálních podmínek je v plynu o objemu 1 cm3 přibližně 3 . 1019 molekul. Molekuly dusíku mají průměr 2r
 3 . 10-10 m a střední rychlost
3 . 10-10 m a střední rychlost
 4,5 . 102 m . s-1. Srážková frekvence je potom
4,5 . 102 m . s-1. Srážková frekvence je potom
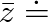 4 . 109 s-1.
4 . 109 s-1.
Známe-li srážkovou frekvenci, můžeme vypočítat střední volnou dráhu
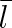 , což je průměrná délka trajektorie, na níž nedojde ke srážce molekuly. Za jednotku času proletí molekula dráhu číselně rovné
, což je průměrná délka trajektorie, na níž nedojde ke srážce molekuly. Za jednotku času proletí molekula dráhu číselně rovné
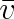 , přitom dojde v průměru k z srážkám, takže platí
, přitom dojde v průměru k z srážkám, takže platí
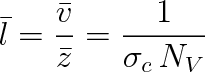 |
(6.6) |
Pro dusík za normálních podmínek je
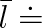 1 . 10-7 m.
1 . 10-7 m.
Střední volná dráha se mění nepřímo úměrně s tlakem plynu p (p ~ NF).
Podle výrazu (6.6) je střední volná dráha nezávislá na teplotě.
Přesnější úvahy ukazují, že účinný průřez závisí na střední rychlosti, a tím i na teplotě T. Tato závislost účinného průřezu se často vyjadřuje Sutherlandovým vzorcem
 |
(6.7) |
Veličiny
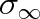 a K jsou empirické konstanty, které se pro jednotlivé plyny určují z experimentu. Veličinu
a K jsou empirické konstanty, které se pro jednotlivé plyny určují z experimentu. Veličinu
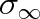 je možno považovat za účinný průřez při vysokých teplotách.
je možno považovat za účinný průřez při vysokých teplotách.