Třetí termodynamický zákon se týká termodynamických stavových funkcí a vlastností látek za teplot blízkých 0 K. Podle W. H. NERNSTA (Němec, 1864-1841) je při libovolném izotermickém ději při teplotě 0 K změna entropie soustavy
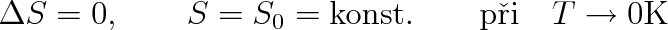 |
(4.26) |
nezávislá na změnách jiných stavových veličin. Z toho plyne, že při 0 K se izotermický děj stává současně dějem izentropickým.
Třetí termodynamický zákon se dále týká dosažitelnosti teploty 0 K. I když se již podařilo přiblížit se k teplotám řádově až 10-6 K, podrobný rozbor experimentů prováděných v těsném okolí 0 K ukázal, že zkoumanou látku nelze konečným počtem dějů ochladit na teplotu 0 K.
Zkončením těchto poznatků je formulace: Žádným postupem, ať jakkoli idealizovaným, nelze u žádné soustavy dosáhnout snížení její teploty na hodnotu 0 K konečným počtem operací.
Důsledkem definičního vztahu (4.26) je, že měrné tepelné kapacity cp a cV se pro T
 K rovnají nule. Pro změnu entropie totiž platí (viz vztahy (4.13) a (3.15)), že
K rovnají nule. Pro změnu entropie totiž platí (viz vztahy (4.13) a (3.15)), že
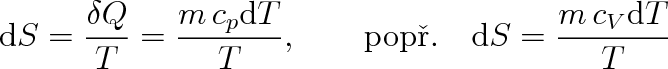 |
Aby tyto výrazy pro T
 0 K byly rovny nule, musí platit
0 K byly rovny nule, musí platit
 |
Kromě měrných tepelných kapacit se při teplotě 0 K rovnají nule i všechny teplotní součinitelé (např. roztažnosti).